背景 これまで行われてきた製造販売後調査、安全性情報報告は、使用実態や結果が遅滞なく使用者にもたらされず、費用と労力に見合う成果がもたらされていないという意見がある。
概要 2018年に改正された省令で追加された「製造販売後データベース調査」に基づき、GPSP省令が適用される新医療機器、学会が登録を要すると定めた医療機器、主に有害事象を中心に使用成績を調査することを要すると判断する新規医療機器を対象として、本学会が実施症例のデータを収集し、企業はそれを活用して当局に報告し公表する。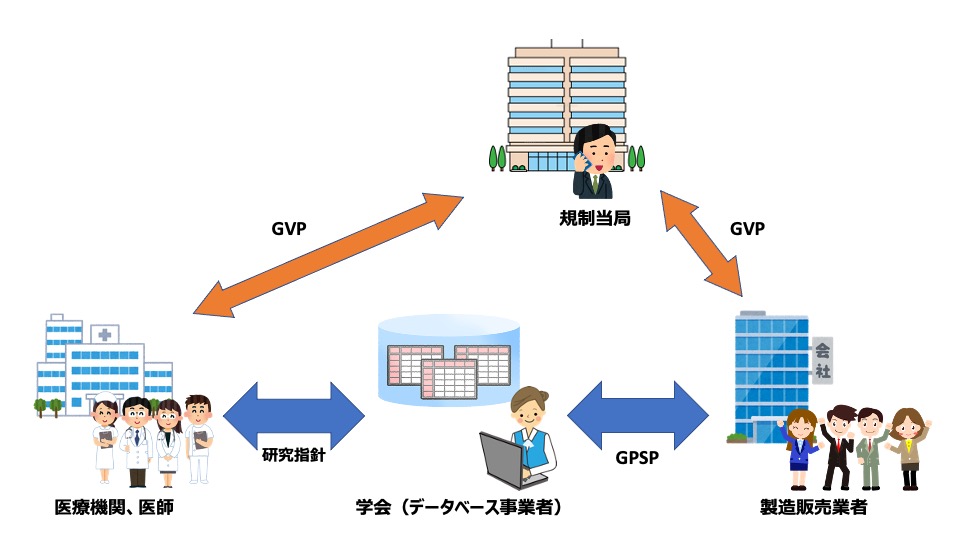



事業
分岐部脳動脈瘤PMS
対象機器 PulseRider(ジョンソンエンドジョンソン)、W-EB(テルモ)
期間 2020年7月開始
情報ページへ
入力ページへ(参加者専用)
Pipeline PREMIER PMS
対象機器 Pipeline Flex with Shield Technology(メドトロニック)
期間 2021年3月開始
情報ページへ
入力ページへ(参加者専用)
Surpass Streamline PMS
対象機器 Surpass Streamline(ストライカー)
期間 2021年10月開始
情報ページへ
入力ページへ(参加者専用)
組織
組織体制
日本脳神経血管内治療学会 データベース事業運営委員会委員
宮地 茂 (NPO法人日本脳神経血管内治療学会理事長、データベース取扱事業者長)
松丸祐司 筑波大学 脳神経外科脳卒中予防・治療学講座(同事務局長、委員長)
小林繁樹 自動車事故対策機構 千葉療護センター
神山信也 埼玉医科大学国際医療センター 脳神経外科
坂井千秋 京都大学 脳神経外科
坂井信幸 医療法人清仁会シミズ病院 脳神経外科
滝川知司 獨協医科大学埼玉医療センター 脳神経外科
根木宏明 浜松医科大学医学部附属病院 脳神経外科
問い合わせ
NPO法人日本脳神経血管内治療学会 データベース事業事務局
〒160-0016 東京都新宿区信濃町35 信濃町煉瓦館5F 一般財団法人国際医学情報センター内
jsin-office@umin.ac.jp


